A bélflóra szerepe az egészségben és a betegségek megelőzésében
Miért hallunk egyre többet a mikrobiom vizsgálatokról és a bélflóráról?
(olvasási idő rövid változat 8 perc, hosszabb változat 10 perc)
Az emberi testben lezajló biokémiai folyamatokról az orvostudomány rengeteg információval rendelkezik. Közismert tény, hogy az emberi test nem steril, és hogy mikroorganizmusokkal osztozunk a szervezetünkön, főleg a bőrön, szájüregben, belekben, légzőrendszerben, húgyutakban és a hüvelyben. Egy átlagos esetben több milliárd (~100 billió – 1012) baktérium, gomba, vírus és archea (ősi egysejtű élőlény) él velünk, és ezek 95 %-a a bélrendszerünkben található (1). Ezen organizmusok közül a baktériumok kapták a legnagyobb figyelmet, és a vizsgálatok is elsősorban ezeket mutatják ki hatékonyan.
Minden baktérium faj egy különálló életforma és egyedi élettani folyamatok zajlanak le bennük. Ezek a biokémiai folyamatok hatással vannak az emberre is, pl. vitaminokat és hasznos tápanyagul szolgáló rövid láncú zsírsavakat biztosítanak a testnek. Egyes fajok azonban gyulladáskeltő és bélfal sérüléseket okozó anyagokat is kibocsáthatnak magukból, amelyek komoly egészségügyi problémákat jelenthetnek, és hosszú távon akár daganatok kialakításában is részt vehetnek.
Beleszólhatnak a cukoranyagcserébe, az idegsejtek működésbe, de képesek szabályozni a testsúlyunkat is. Amikor egy-egy velünk élő organizmus ekkora befolyással van ránk, akkor hasznos, ha tudomást szerzünk a jelenlétükről, mert válaszokat kaphatunk a szervezetünkre ható, eddig akár rejtettnek tűnő problémák okaira is.
Ha az egész testünket körbe veszi a mikrobiom - kívül és belül is - mi az oka annak, hogy a vastagbél flórjával foglalkozunk mégis a legtöbbet?
Mert itt található az immunrendszerünk 80%-a! Ez a terület egy különleges védelmi központ, amit GALT-nak hívunk (gut-associated lymphoid tissue). A bélfal mögötti kötőszövet, azaz a lamina propria az immunsejtek otthona – itt dönti el a szervezet, hogy harcoljon vagy toleráljon egy adott hatást.
A mikrobiom segíti az immunrendszert abban, hogy felismerje: mi ártalmas és mi nem. Itt történik például a naiv T-sejtek átalakulása védekező vagy nyugtató (reguláló) immunsejtekké – és ez a folyamat a mikrobák által termelt anyagoktól (mint a rövid láncú zsírsavak, főleg a vajsav) és a retinoltól (A-vitamin) is függ.
A legtöbb fertőzés a nyálkahártyán keresztül jut be a szervezetbe – ezért itt, a bélrendszerben van a legnagyobb szükség jól működő védelemre. A vastagbél mikrobiomja nem csak segít megvédeni minket a kórokozóktól, hanem abban is, hogy ne legyen túlzott az immunválasz – például allergia vagy autoimmun reakció formájában.
Szóval, ha tudni akarjuk, mivel küzd a szervezetünk, először azt kell tudnunk, kikkel élünk együtt – mert ez a láthatatlan ökoszisztéma a legfontosabb védelmi bástyánk!
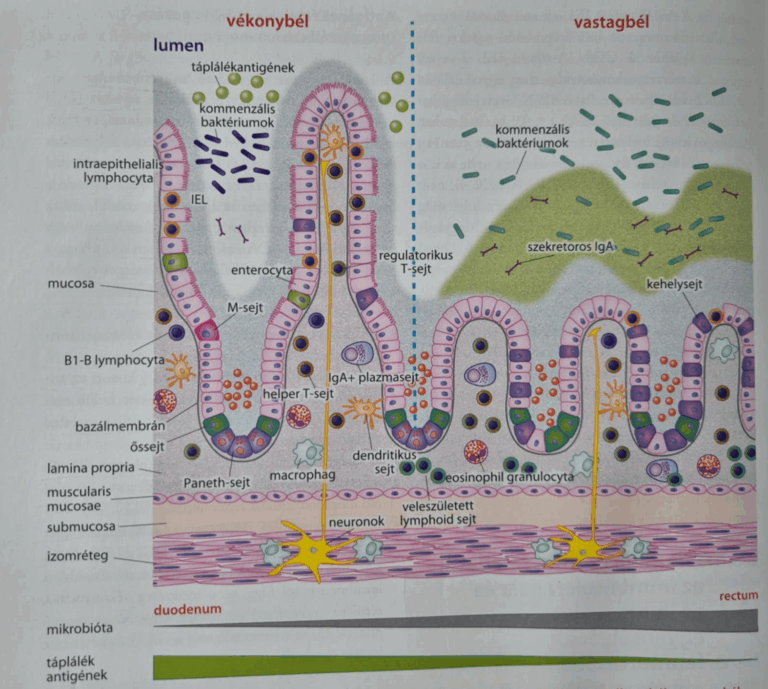
Lamina propria (Tulassay Zsolt, Gasztroenterológia, 2023)
Mit tudhatunk meg egy mikrobiom vizsgálat során?
Információkat szerezhetünk a bélfalat védő nyálka állapotáról, a kellemetlen tüneteket is provokáló gázok termeléséről, a rövid láncú zsírsavak arányáról (ezek tápanyagot szolgáltatnak a bélfal sejtek, immunsejtek, máj, agy, izmos számára), az idegrendszert támogató vagy irritáló anyagcsere termékekről, a jelen lévő kórokozókról, illetve az azok ellen védő fajokról vagy védő anyagokról (mint például a tejsav), a hisztamin termelésről, de akár a gyulladásos folyamatokról, sőt, még a daganat indító hatással bíró fajokról is. Ha ezekről részletesebben szeretnél olvasni, kérlek, nyisd meg az alábbi címeket!
A bélfalat védő nyálka, a mucin réteg támogatása
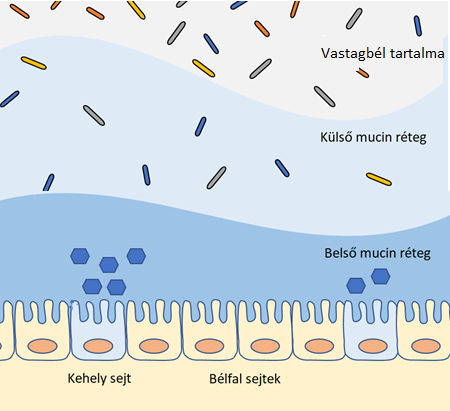
A mucin egy 2 rétegű nyálka (lásd a lent csatol sematikus ábra), amelynek a bélfal felé eső része sűrű és kemény, védi a beleket a baktériumok bejutásától. A bélfal ürege felé eső része pedig puha, és a bélflóra baktériumainak ad otthont. A megfelelő működéshez ennek a rétegnek mindig frissnek, és optimális vastagságúnak kell lennie. Azért, hogy ez az egyensúlyi állapot meg tudjon valósulni, folyamatosan frissíteni kell ezt a réteget – egyes fajok a mucin termelését támogatják, más fajok pedig ezt a mucint eszik meg, és ezzel arra késztetik a bélfalban lakó mucin termelő sejteket, hogy több mucint termeljenek. Ennek a folyamatnak a szabályozását is egy baktérium (Akkermansia muciniphila) végzi.
Jelentős mennyiségben lehetnek jelen olyan fajok a bélflórában, amelyek gázokat termelnek. A kénhidrogén gáz kellemetlen szagú, ilyenkor fordulhatnak elő a kénes, savanyú szagú szelek. A kellemetlen szag maga nem káros, de ezek a gázok képesek roncsolni a bélfal sejtek genetikai állományát, egyes fajok képesek komoly gyulladásos folyamatokat elindítani (3).
A metán gáz képes a bél mozgásait korlátozni (4), emiatt tovább maradhat a széklet a vastagbélben, így több vizet szív ki belőle a szervezet. Ezzel kemény állagú széklet jöhet létre, ami gyakran székrekedést idézhet elő és aranyér problémákat okozhat hosszú távon.
Az ammónia gáz nagy mennyiségben képes károsítani a májat (5), amely elsősorban a fehérjék vékony- (5) és vastagbélen (6) való bontásából származik.
A vastagbélben élő baktériumok különböző anyagcsere termékeket választanak ki. Ezek egyik csoportja a szervezet számára tápanyagul szolgáló rövid láncú zsírsavak – SCFA (angolul: short chain fatty acid). (7) A legjelentősebb hatású zsírsavak az acetát (vagy ecetsav), a propionát (vagy propionsav) és a butirát (vagy vajsav) – mennyiségük a felsorolás mentén, egészséges emberek vastagbelében a következő arányban van jelen: 60:20:20.
Az ecetsav nagyon fontos a testsúly szabályozásában, a máj és az agy támogatásában. A tudomány jelenlegi állása szerint az ecetsav pozitív hatását gyakorol az emberi szervezetre.(8)
A propionsav nagyon fontos a cukoranyagcsere, az izommunka és a máj támogatása szempontjából. Hiányában az izmok és máj nem tudnak tökéletesen működni, többlete esetén pedig az idegrendszert tudja terhelni, illetve negatívan befolyásolhatja a cukoranyagcserét. (9)
A vajsav vagy butirát első sorban a bélfal sejteket és egyes immunsejteket táplálja, ezzel képes a gyulladásokat csökkenteni. Egyes sejtek növekedését is képes gátolni, ezzel rákellenes hatást gyakorol. Ha túl sok termelődik belőle, akkor egyes esetekben tovább ronthat a gyulladt bélfal állapotán, mert meggátolhatja, hogy a bélfal őssejtjei érett bélfal sejtekké alakuljanak – ezt a folyamatot hívjuk butirát paradoxonnak. (10)
A “bélagy” és a “bél-agy-tengely” ma már közismert kifejezések. Az emésztőrendszer saját idegrendszerrel rendelkezik (enterális idegrendszer), és az agyunk közreműködése nélkül is képes levezényelni az emésztés folyamatának legnagyobb részét. Vannak baktériumok a vastagbélben, amelyek a bél idegsejtjeinek egymással való kommunikálását tudják befolyásolni – egyesek pozitív, mások negatív irányba. Ahogy a bél-agy-tengely kifejezés jelzi, az agyunk és az emésztőrendszerünk idegrendszere aktív kapcsolatban van egymással, így ezek a baktériumok a központi idegrendszerünkre is hatással lehetnek, így az emésztőrendszeri és neurológiai problémák mellett pszichés gondokat is előidézhetnek. Egyes bélbaktériumok olyan idegsejtek közötti kommunikációs anyagok (neurotranszmiter) termelést tudják közvetve vagy közvetlenül befolyásolni, mint pl. a szerotonin, dopamin, hisztamin, GABA, stb. (11)
Egy bélrendszeri fertőzésre az agyunk is reagál (12), emiatt idegrendszeri tüneteket is okozhatnak a kórokozók.
Egyes baktériumok képesek elősegíteni a szervezet védekezését a kórokozó fajokkal szemben: csökkentik a gyulladást, támogatják a védő nyálka termelést, versengenek a helyért és a táplálékért. Közvetlen módon is képesek beleszólni a patogének elleni védekezésbe antimikrobiális hatású anyagokat termelve. Ilyenek lehetnek az Escherichia coli probiotikus törzsei, például az Escherichia coli Nissle 1917. (13) (14)
A vastagbél flóra egyes tagjai – főleg a probiotikus hatásaikról ismert Lactobacillusok és Bifidobacteriumok – szénhidrátok fermentálásával sok hasznos anyagot termelnek, köztük tejsavat, azaz laktátot. A tejsav és egyéb, bacteriocinnek nevezett anyagcsere termékek antimikrobiális hatásúak, megakadályozzák egyes kórokozó baktérium szaporodását 15). A tejsav másik fontos tulajdonsága, hogy vegyhatásának köszönhetően részt vesz a vastagbél savas környezetének kialakításában, ami inkább a hasznos baktériumoknak kedvez, mert a patogének többsége a lúgosabb pH-t preferálja.
Hisztamintermelés a vastagbélben
A hisztamint az emberi szervezet aminosavakból képes előállítani, és nagyon sok élettani folyamat során tudja azt hasznosítani: immunvédekezés, gyomorsav termelés, éberség szabályozása stb. Az utóbbi időben rossz színben tüntették fel ezt a szervezet számára nélkülözhetetlen anyagot. A bélflóra által termelt hisztamin vélhetően csak akkor fog gondot okozni, ha abból nagyon sok termelődik, és a szervezet nem tudja a felesleget lebontani. (16). A fel nem használt és le nem bontott hisztamin nagy mennyiségben lesz jelen, és így allergiához hasonló tüneteket képes provokálni a szervezetben.
A kórokozó (patogén) fajok a baktérium közösség egy tudományos igénnyel meghatározott csoportja, amely jelenlétével betegségeket tud előidézni. Ilyen fajok például: Campylobacter jejuni, Clostridioides difficile, Shigella nemzetség tagjai, Staphylococcus aureus, Escherichia coli, Vibrio cholerae, Yersinia enterocolitica (17).
Virulencia faktorok – A virulencia faktor a baktériumok vagy más kórokozók által termelt anyag, amely fokozza a fertőzőképességet és elősegíti a betegség terjedését, serkenti a kórokozó szaporodását, vagy gyengíti a megtámadott szervezetet (18), a test adott felületéhez való tapadását, mechanikai védelmét, méreganyag termelését (toxinok), pórus képzést a sejtfalon stb. (19).
Daganat indító, vagy daganatos állapotokat kedvelő fajok
Léteznek olyan fajok, amelyekről a tudomány már bebizonyította, hogy képesek daganatos folyamatokat elindítani a vastagbélben vagy a test más részein. Ilyen fajok például a Fusobacterium nucleatum és Bacteroides fragilis (ennek csak a fragizin nevű virulencia faktort tartalmazó változatai) (20), vagy akár a Parvimonas micra (21), stb.
Az öreg barát elmélet - avagy hogyan élhetünk együtt baktériumokkal, anélkül, hogy megbetegednénk vagy belehalnánk?
Erre az öreg barát elmélet (23) adja meg a választ – az ember törzsfejlődése ezekkel a baktériumokkal együtt élve történt meg, együttesen hoztuk létre az emberi szervezet mai ismert élettani folyamatait. Az immunrendszerünk ismeri ezeket a fajokat, és a jelenlétük nem vált ki az immunsejtekből olyan választ, amely a baktériumok elpusztítását eredményezné.
Létezik-e jó vagy rossz baktérium?
A baktériumok nem jók vagy rosszak, hanem egyedi életformák, és mint minden más élőlény, küzd a fennmaradásáért. Az, hogy az ő életfolyamataik pozitívan vagy negatív hatnak az emberi egészségre, azt sok tényező befolyásolja. Vannak kórokozók, azaz patogének, amelyek jelenléte már önmagában veszélyt jelent az egészségre – ezek egyértelműen “rossz” baktériumok. Ugyanakkor egyes fajok a létezésükkel támogatják a szervezetet, tápanyagokat termelnek, és ezért az úgynevezett “jó” vagy “hasznos” baktériumok közé soroljuk őket.
Azonban néha a “hasznos” fajok is okozhatnak gondot, elsősorban akkor, ha túlszaporodnak a bélflórában, károkat okozva a szervezetnek az anyagcsere termékeikkel – lsd. butirát paradoxon.
Milyen tényezők játszanak szerepet a bélflóra összetételében?

Ha röviden akarunk válaszolni: az életvitelünk szinte minden tényezője.
Étkezés – A vastagbélben élő baktériumok legtöbbször közvetlenül azt eszik, amit mi. Az étkezéssel ezért közvetlenül befolyásolni tudjuk a bélflóránk összetételét.
Változatosság vagy éppen annak a hiánya – Ha rendszeresen ugyanazt fogyasztjuk, akkor mindig ugyanazokat a baktériumokat tápláljuk. Ha változatos bélflórát szeretnénk, változatosan kell étkeznünk.
Alkoholfogyasztás – A tapasztalatok szerint a nagy mennyiségben fogyasztott alkohol képes elősegíteni egy olyan bélflóra kialakulását, amely károsíthatja a bélfal sejtjeit, és daganatos folyamatokat indíthat meg hosszú távon.
Szorongás – Szorongás közben az idegrendszerünk “harcolj vagy menekülj” helyzetre készíti fel a szervezetet. Nyilvánvaló, hogy sem harc sem menekülés esetén nem előnyös, ha tele van a hasunk. Ha nem emésztünk megfelelően, akkor az emésztetlen étel-többlet a vastagbélben lévő baktériumokat fogja táplálni, és így akár rossz irányba is változtathatja a bélflóra állapotát.
Fertőzések – Életünk során rengeteg kórokozóval nézünk szembe. Ezek nagy részét már a bőrön, az orr és a száj nyálkahártyáján elpusztítja az immunrendszerünk. Egyes kórokozók azonban elérik a vastagbelet, és ezzel komoly károkat okozhatnak, például napokig tartó vizes vagy akár véres hasmenést, gyulladásokat, bélfal sejtek elhalását, vagy extrém esetekben – a nyugati világban szerencsére ritkán – halálhoz is vezethetnek.
Az antibiotikumok gyakori használata – Mivel az antibiotikumokat a baktériumok elpusztítására fejlesztették ki, ezért természetes, hogy a bélben élő baktériumokra is hatással vannak.
A bélflóra és más testrészek mikrobiomjának kapcsolata
Rendszeresen tapasztaljuk azt, hogy a száj, a hüvely, és vélhetően a húgyutak normál vagy patogén flórája is jelen van a vastagbélben. Emiatt egyes esetekben fogorvos, nőgyógyász, urológus felkeresését javasoljuk.
Melyek az első lépések a bélflóra regenerálása során?
A regenerálás folyamata mindig attól függ, hogy milyen fajokat azonosítanak a vastagbélben.
Patogének esetén mindig felhívjuk a figyelmet arra, hogy első körben szakorvossal kell egyeztetni a problémáról.
Az általunk kínált megoldások, személyre szabva, növényi hatóanyagokat, probiotikumokat, szelektív hatású rostokat és egyéb prebiotikumokat, valamint gyulladáscsökkentő hatóanyagokat tartalmaznak.
Hogyan tartható fenn hosszú távon a bélflóra egészsége?
Az egészséges bélflóra kulcsa a változatos étkezés, természetes probiotikumok (fermentált és érlelt ételek) és növényi rostok fogyasztása. Kiemelten fontos az emésztőrendszer felsőbb szakaszainak (pl. fogak, gyomor, vékonybél) egészsége is, mert csak így juthat megfelelően megemésztett és kórokozóktól fertőtlenített étel a vastagbélbe.
Rostok
A rostok olyan összetett szénhidrátok, amelyeket a hasnyálmirigy által termelt szénhidrát emésztő enzim, az amiláz, nem képes lebontani, így érintetlen formában érik el a vastagbelet. Ilyen rostok például: inulin, galacto-oligoszacharid (GOS), fructo-oligoszacharid (FOS), xilo-oligoszacharid (XOS), kito oligoszacharid, rezisztens keményítő, fulvosavak, huminsavak, stb.
Hasznos-e számomra, ha rostot eszek?
A rostok pozitív hatásai:
- hasznos baktériumokat táplálnak a vastagbélben
- tartalmat és súlyt adnak a székletnek, gyorsíthatják a tranzit időt ezzel megakadályozzák a székrekedést
A rostok esetleges negatív hatásai:
- puffadást idézhetnek elő a vékony- és/vagy vastagbélben
- irritálhatják a beleket, fájdalmat okozhatnak bélgyulladás esetén
- támogatják egyes fajok túlszaporodását a vastagbélben, ezzel kibillentik a bélflóra egyensúlyát
- gyorsíthatják a tranzit időt, így az étel gyorsabban áthalad a bélrendszeren, ezzel hasmenést okozva

Szelektív rostok
A szelektív rost olyan rost, amely csak meghatározott baktérium fajokat tud táplálni. Az ilyen típusú rostokkal irányított módon tudunk előnybe hozni egyes növelni kívánt fajokat más fajokkal szemben. A bélflóra regenerálása során nagyon fontos, hogy elsősorban ilyen szelektív rostokkal dolgozzunk, hogy a célzott baktérium csoportok növekedését tudjuk befolyásolni.
Milyen esetben érdemes mikrobiom vizsgálatot kérni?
Gyomor- és bélrendszeri problémák esetén
🌬️ Puffadás, hasi görcsök
💨 Szelesedés – főleg amikor kellemetlen szagúak a szelek
🧬 Bélgyulladásnál (IBD) – Crohn, Colitis ulcerosa, proctitis, proctocolitis
🧪 Magas calprotectin érték
🩸 Látható véres széklet vagy laboratóriumban kimutatott székletvér
🚽 Gyakori hasmenés vagy rendszeres híg széklet
🪨 Székrekedés vagy rendszeres, de nagyon kemény állagú széklet
❓ IBS, egyéb, nem ismert eredetű hasi panasz, ismeretlen eredetű hasi fájdalom
🥛 Ételintoleranciák, felszívódási zavarok
Hormonális és női problémák esetén
🦋 Pajzsmirigy problémák
⚙️ PCOS, endometriózis
🩸 Menstruációs zavarok
🌱 Funkcionális meddőség
💧 Ösztrogén többlet
🍬 Inzulinrezisztencia, cukorháztartás zavarai
🌑 Pattanásos bőr
Pszichés és neurológiai problémák esetén
🧠 Depresszió, szorongás
🎯 Viselkedési és figyelemzavarok, ADHD
🧩 Autizmus, autisztikus tünetek
⚡ TIK zavarok
🌪️ Ismeretlen eredetű fejfájások
Ismeretlen eredetű fertőzések esetén
🌍 Külföldi utazásról visszatérve furcsa hasi panaszok
🔬 Klasszikus tenyésztési vizsgálattal nem kimutatható fertőzések
🦠 Krónikus vírusfertőzések
🧫 Krónikus bakteriális fertőzések
Egyéb panaszok esetén
⚖️ Hízás vagy fogyás nehézsége
🧴 Bőrproblémák
🛡️ Immunhiány jelei, visszatérő fertőzések, autoimmun betegségek
🔥 Krónikus gyulladások vagy hisztaminintolerancia
Hogyan vizsgálják ma a mikrobiomot? Van-e különbség a genetikai vizsgálatok információ tartalma között?
Klasszikus klinikai mikrobiológia
A folyamat során specifikus táptalajra kennek mintákat (pl. széklet, vagy egyéb testváladékok), és megvizsgálják, hogy növekedésnek indult-e rajtuk az adott táptalajon élő baktérium.
Ennek a módszertannak több korlátja is van, például, hogy a bélflórában lakó baktériumok nagy része nem életképes oxigéndús környezetben (ezek az úgynevezett anaerob baktériumok), és ezek akár percek alatt képesek elpusztulni szabad levegőn. A másik kritikus pont, hogy a klinikai mikrobiológus szakember nem azt vizsgálja, hogy milyen baktérium van jelen a mintában, hanem azt, hogy az a baktérium, amit ő keres, jelen van-e az adott mintában.
Genetikai vizsgálatok
A genetikai vizsgálatok kevésbé függenek az emberi tényezőtől. A mintavétel során olyan tartósító anyagot használnak a laborok, amely konzerválja a széklet állapotát, így az oxigéndús levegő nem öli meg a baktériumokat.
A 16S rRNS módszertan (metataxonómia) elsősorban baktérium nemzetségeket tud megkülönböztetni, és csak korlátozottan képes a baktérium fajokat kimutatni a székletmintákból.
A Shotgun módszertan (metagenomika) a mintákban található legtöbb baktérium fajt képes kimutatni, így (a Nature-ben megjelent publikáció szerint (25)) sokkal pontosabb információt ad a bélflóra állapotáról, mint a 16S rRNS módszertan.
Mi a PSYBIOM-nál a Shotgun módszertannal dolgozunk.
Létezik-e konkrét betegségekre jellemző bélflóra mintázat?
A kutatások során felfigyeltek arra, hogy bizonyos betegségek esetén szignifikánsan nagy arányban vannak jelen meghatározott baktérium csoportok.
Mennyire van alátámasztva tudományosan a bél mikrobiom szakterülete?
Erre a kérdésre a legjobb választ talán az alábbi képpel tudjuk megadni: ha rákeres valaki az orvosi területeken végzett kutatásokat gyűjtő adatbázisában (PubMed), akkor több mint 59 000 anyagot talál ebben a témában, melyek nagy része az elmúlt évtizedben született.
Szerző: Lányi Kata
- Gasztroenterológia – 2023. Medicina Kiadó, szerk. Tulassay Zsolt, 120. old. Mikroorganizmusok az emberi szervezetben, Dr. Szabó Dóra.
- https://www.lucymailing.com/scfas-part-2-the-benefits-of-butyrate/
- A human stool-derived Bilophila wadsworthia strain caused systemic inflammation in specific-pathogen-free mice, Zhou Feng, Wenmin Long, Binhan Hao, Ding Ding, Xiaoqing Ma, Liping Zhao, Xiaoyan Pang (PMID: 29090023, PMCID: PMC5657053, DOI: 10.1186/s13099-017-0208-7 )
- The effects of methane and hydrogen gases produced by enteric bacteria on ileal motility and colonic transit time, J Jahng, I S Jung, E J Choi, J L Conklin, H Park (PMID: 22097886, DOI: 10.1111/j.1365-2982.2011.01819.x )
- Gut ammonia production and its modulation – Manuel Romero-Gómez, María Jover, J Jorge Galán, A Ruiz (PMID: 19067141, DOI: 10.1007/s11011-008-9124-3 )
- Ammonia production by human faecal bacteria, and the enumeration, isolation and characterization of bacteria capable of growth on peptides and amino acids, Anthony J Richardson, Nest McKain & R John Wallace, BMC Microbiology
- https://www.lucymailing.com/scfas-part-1-a-brief-introduction-to-short-chain-fatty-acids/
- https://www.lucymailing.com/scfas-part-4-does-acetate-make-you-fat/
- https://www.lucymailing.com/scfas-part-5-the-propionate-autism-connection/
- https://www.lucymailing.com/scfas-part-3-decrypting-the-butyrate-paradox-can-excess-butyrate-be-toxic/
- Gasztroenterológia – 2023. Medicina Kiadó, szerk. Tulassay Zsolt, 22. old. Dr. Dóra Dávid, A bél-agy tengely
- Gasztroenterológia – 2023. Medicina Kiadó, szerk. Tulassay Zsolt, 125-126. old. Mikroorganizmusok az emberi szervezetben, Dr. Szabó Dóra.
- Antibacterial MccM as the Major Microcin in Escherichia coli Nissle 1917 against Pathogenic Enterobacteria – https://www.mdpi.com/1422-0067/24/14/11688
- Dezfulian A., Ardekani A., Aslani M.M., Dabiri H., Zali M.R. Influence of the probiotic Escherichia coli strain Nissle 1917 on the growth of different pathogenic bacteria isolated from patients with diarrhea. Gastroenterol. Hepatol. Bed Bench. 2008;1:113–117
- Bacteriocin-Producing Probiotic Lactic Acid Bacteria in Controlling Dysbiosis of the Gut Microbiota, Anjana, Santosh Kumar Tiwari,
- https://www.healways.hu/hisztamin-intolerancia
- https://semmelweis.hu/nepegeszsegtan/files/2019/03/1819_II_AOKgy04_Enter%C3%A1lis-fert%C5%91z%C3%A9sek.pdf
- http://patikapedia.hu/virulencia-faktor
- https://semmelweis.hu/mikrobiologia/files/2014/09/FOK_02.pdf
- Gut microbiota in colorectal cancer: mechanisms of action and clinical applications, Sunny H. Wong & Jun Yu, Nature Reviews Gastroenterology & Hepatology volume 16, pages 690–704 (2019)
- Tumour Colonisation of Parvimonas micra Is Associated with Decreased Survival in Colorectal Cancer Patients, Thyra Löwenmark, Anna Löfgren-Burström, Carl Zingmark, Ingrid Ljuslinder, Michael Dahlberg, Sofia Edin, Richard Palmqvist, Ikuko Kato (doi: 10.3390/cancers14235937, PMCID: PMC9736682, PMID: 36497419)
- https://www.daganatoserek.hu/vastagbelrak-es-vegbelrak-stadiumok-es-kezelesek/
- The old friends hypothesis: evolution, immunoregulation and essential microbial inputs Graham A W Rook
- https://www.vital.hu/alkoholista_kategoriak_alkohol
- Comparison between 16S rRNA and shotgun sequencing data for the taxonomic characterization of the gut microbiota, Francesco Durazzi, Claudia Sala, Gastone Castellani, Gerardo Manfreda, Daniel Remondini & Alessandra De Cesare, Scientific Reports volume 11, Article number: 3030 (2021)
- https://pubmed.ncbi.nlm.nih.gov/?term=gut+microbiome

